10月23日,生物制药企业Celltrion的Zymfentra (infliximab-dyyb,英夫利西单抗)的皮下注射剂获得FDA批准,这是英夫利西单抗的首个皮下注射剂型,用于治疗炎症性肠病(IBD)。Zymfentra预计于2024年第一季度上市,在上市前,公司不会公布产品价格。
此次FDA批准基于Celltrion两项III 期试验的积极数据,这两项试验评估了英夫利西单抗用于维持治疗中度UC (LIBERTY-UC) 和CD (LIBERTY-CD) 患者的有效性和安全性。
根据LIBERTY UC和LIBERTY CD两项研究的结果,与安慰剂相比,在患者接受静脉注射英夫利西单抗诱导治疗的第54周时,Zymfentra组在临床缓解(UC和CD)(分别为43.2%>20.8%,62.3%>32.1%)和内镜反应(CD)(51.1% >17.9%)的主要终点方面表现出临床优越性。同时,在治疗期间,Zymfentra组的总体安全性与安慰剂相似,未发生新的安全事件。
IBD是一种病因不明的慢性非特异性肠道炎症性疾病,包括3种主要类型:克罗恩病(CD)、溃疡性结肠炎(UC)和未分型IBD(IBD-U)。IBD在成人中发病率高,但近年来,IBD在儿童中发病率越来越高。作为一种慢性、进行性和复发性的肠道疾病,IBD严重影响患者的生活质量和日常生活,增加医疗负担。根据2022年中金创新药前沿系列研报公布的数据,IBD影响着全球约600万—800万患者。
英夫利西单抗(原研药商品名:Remsima)是一种抗肿瘤坏死因子(TNF-a)单克隆抗体,用于治疗CD、UC、类风湿性关节炎以及强直性脊柱炎等患者。它是Celltrion开发的首个抗体生物类似药,目前已获批用于常规治疗无效的中、重度IBD,是治疗IBD的四种主流生物制剂之一。
2016年4年,英夫利西单抗获得美国FDA的销售许可后,销售额急速增长,2018 Q3单季度的销售额达到9200万美元,2018全年的销售额达6.42亿美元。(数据来源:Bloomberg、光大证券研究所)
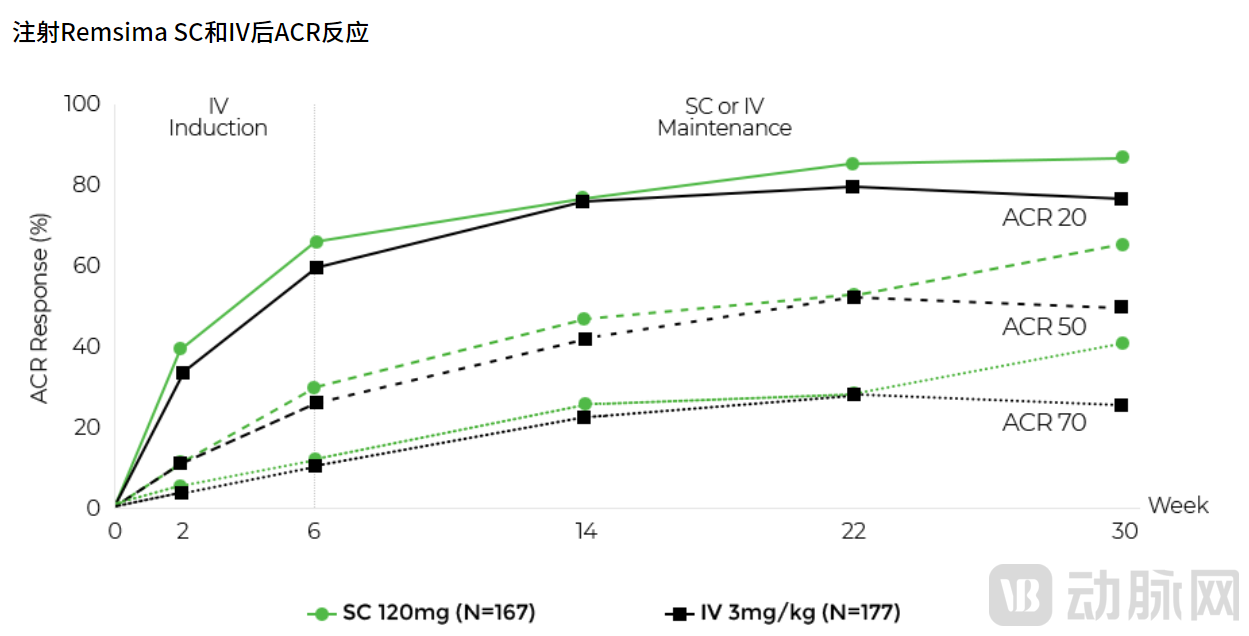
为提高患者用药便利性,Celltrion基于Remsima累积多年的临床结果和患者数据,研发出了克服Remsima IV(静脉注射给药方式)的英夫利西单抗皮下注射剂(原商品名:Remsima SC)。临床试验数据显示,与Remsima静脉注射给药相比,Remsima SC的药物疗效略胜一筹,且有效性和安全性不相上下。
Remsima SC改善了原Remsima的缺点,让患者可自行注射给药,从而减少去医院的次数,提高了患者用药的便利性。同时,新剂型也为医生提供一种替代性的给药选择,克服了TNF-α抑制剂的局限性。
据2022年中金创新药前沿系列研报,当前,IBD全球市场约为180亿美元,预计到2030年全球将增长至约490亿美元。除英夫利西单抗外,阿达木单抗、乌司奴单抗和维得利珠单抗目前是IBD药物市场的主流产品,这四种产品占全球IBD市场收入的75%。
自以阿达木单抗为代表的生物制剂疗法成为IBD患者的治疗新选择后,患者的生存质量得到了很大程度的改善,但目前的疗法仍然存在问题。据美国国立卫生研究院发布的IBD免疫学综述,大约有1/3的患者对生物制剂疗法没有反应,另外约1/2初始治疗有效的患者会发生“继发性反应丧失”现象,类似于抗生素的“耐药”。
面对巨大的市场潜力和未被满足的临床需求,默沙东、辉瑞等巨头纷纷布局IBD赛道,仅2023年,就已经出现了3笔大型交易。其中,TL1A(TNF配体相关分子1A)抗体备受青睐。
TL1A抗体能够针对IBD中的关键病理因子TL1A,从而同时抑制肠道的炎症和纤维化途径,临床证明其安全性和耐受性良好,适用于UC和CD两种类型的IBD,以及可能的肠外表现,如关节炎、皮肤损害等。
4月16日,默沙东以108亿美元收购生物技术公司Prometheus Biosciences,获得其IBD候选治疗药物TL1A单抗PRA-023。PRA-023在临床II期ARTEMIS-UC试验和临床IIa期APOLLO-CD试验的结果表明,其在治疗UC和CD方面具有潜在的安全性和有效性。
10月4日,赛诺菲与梯瓦制药达成合作,以5亿美元预付款和高达10亿美元的开发和里程碑付款,共同开发新型抗TL1A疗法TEV'574。TEV574目前处于II期临床阶段。
10月23日,罗氏宣布以71亿美元收购Roivant子公司Telavant及其IBD候选治疗药物管线RVT-3101。RVT-3101是一种靶向TL1A的全人源单克隆抗体,通过抑制TL1A靶向炎症和纤维化途径,是一种潜在的first-in-class的药物。目前,RVT-3101已在TUSCANY-2期2b研究中对中度至重度UC患者进行了研究,结果显示,RVT-3101具备良好的疗效和安全性。
目前看来,IBD药物的研发远未结束,TL1A已然成为IBD市场的明日之星,但也有企业在进行其他疗法或靶点的创新。
生物制药企业Adiso Therapeutics正在研发一款小分子中性粒细胞调节剂ADS051,用于治疗中度至重度UC。7月13日,Adiso 发表了关于ADS051的临床前研究,并计划于2023年第四季度启动针对UC患者的 2a 期剂量范围临床试验。
此外,10月12日,礼来也宣布了其IBD药物mirikizumab(IL-23单抗)的III期临床试验结果,基于临床数据,礼来将于2024年向FDA提交mirikizumab用于治疗CD的上市申请。








 提供支持
提供支持




















